| Virus BK | |
|---|---|
 |
|
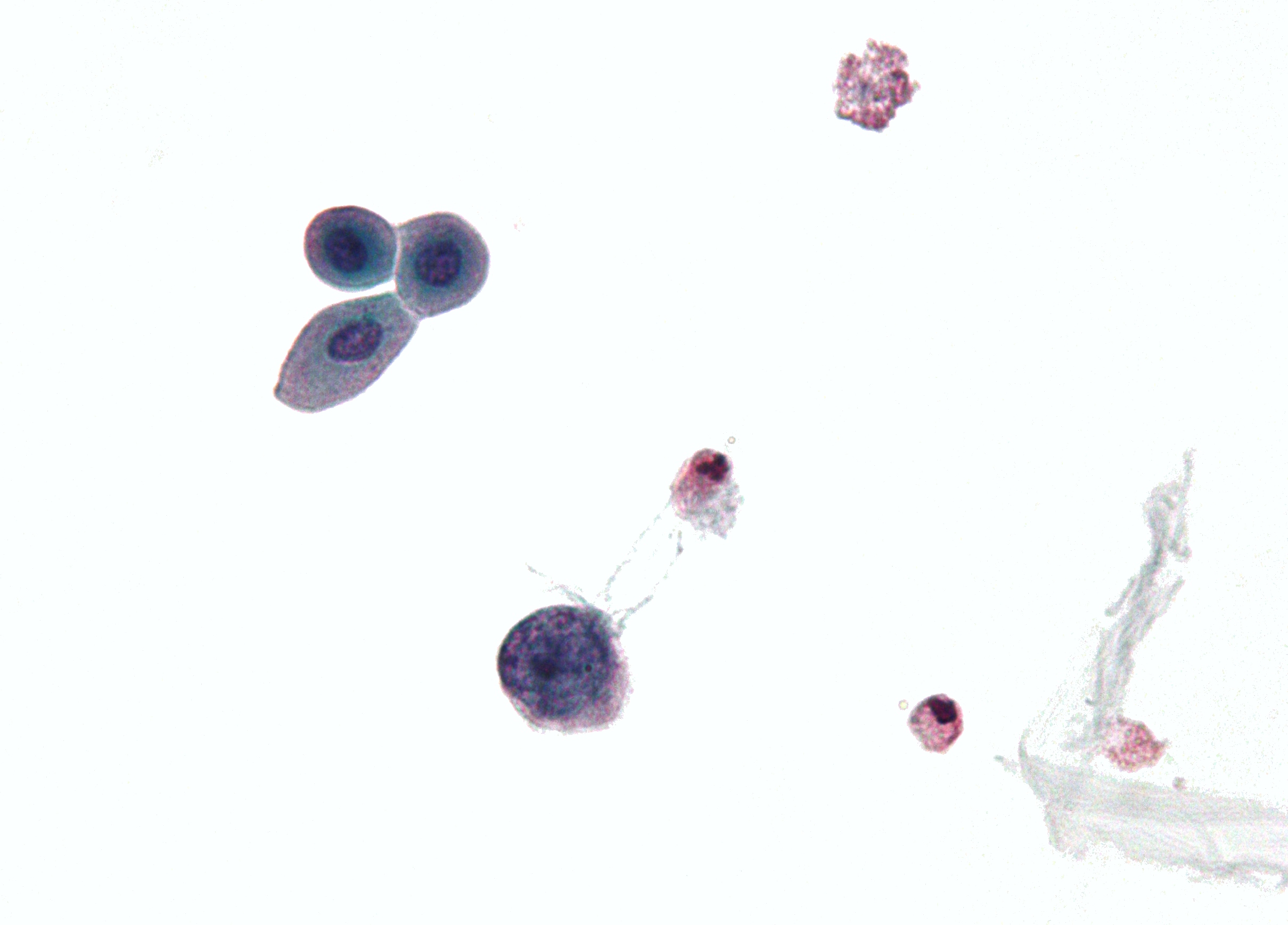
| Micrografia che mostra una cellula infetta da un poliomavirus — grande cellula (blu) in basso al centro-sinistra. Campione di citologia urinaria. | |
| Specialità | Malattie infettive |
Il virus BK è un membro della famiglia dei poliomavirus. L’infezione da virus BK è diffusa, ma conseguenze significative dell’infezione sono poco comuni, ad eccezione degli immunocompromessi e degli immunodepressi. Virus BK è un’abbreviazione del nome del primo paziente dal quale il virus fu isolato nel 1971 (il paziente aveva allora 29 anni).
Sintomi dell’infezione da virus BK
Il virus BK raramente causa malattia ma è tipicamente associato ai pazienti che hanno subito un trapianto di rene; molte persone infette da questo virus sono asintomatiche. Se compaiono sintomi, tendono ad essere lievi: infezione respiratoria o febbre. Questi sono sintomi di infezioni primarie da BK. Anche se senza sintomi clinici, tracce del virus BK sono state rilevate in campioni provenienti da donne colpite da aborto spontaneo. Anticorpi sierici contro il virus BK sono stati trovati anche in donne che hanno subito aborto spontaneo così come in donne che hanno interrotto volontariamente una gravidanza.
Il virus si diffonde quindi ai reni e alle vie urinarie dove persiste per tutta la vita dell’individuo. Si stima che fino all’80% della popolazione contenga una forma latente di questo virus, che rimane latente fino a quando il corpo subisce una qualche forma di immunosoppressione. Tipicamente, ciò si verifica nel contesto di un trapianto di rene o di trapianto multiplo. La presentazione in questi individui immunocompromessi è molto più grave. Le manifestazioni cliniche includono disfunzione renale (visibile tramite un aumento progressivo della creatinina sierica) e un’analisi urinaria anomala che rivela cellule tubulari renali e cellule infiammatorie.
Cause dell’infezione da virus BK
Trasmissione del virus
I medici non sanno come viene trasmesso questo virus. Ma i medici sanno che il virus si diffonde da persona a persona e non da una fonte animale. È stato suggerito che questo virus possa essere trasmesso attraverso fluidi respiratori o urine, poiché gli individui infetti escretano periodicamente il virus nelle urine. Un’indagine su 400 donatori di sangue sani ha mostrato che l’82% era positivo per IgG contro il virus BK.
Fattori di rischio
In alcuni pazienti trapiantati renali, l’uso necessario di farmaci immunosoppressori ha come effetto collaterale quello di permettere al virus di replicarsi all’interno del innesto, una malattia chiamata nefropatia BK.
Dal 1 al 10% dei pazienti trapiantati renali progrediscono verso nefropatia associata al virus BK (BKVAN) e fino all’80% di questi pazienti perdono i loro innesti. L’insorgenza della nefrite può verificarsi già a pochi giorni dal trapianto fino a 5 anni dopo.
È inoltre associata a stenosi ureterale e nefrite interstiziale. Nei destinatari di trapianto di midollo osseo è notevole come causa di cistite emorragica.
Un carico di viremia BK > 185.000 copie/ml al momento della prima diagnosi positiva di BKV è stato considerato il miglior indicatore per BKVAN (97% di specificità e 75% di sensibilità). Inoltre, i picchi di carico virale BKV nel sangue raggiungenti 223.000 copie/ml in qualsiasi momento sono stati trovati predittivi per BKVAN (91% di specificità e 88% di sensibilità).
Diagnosi dell’infezione da virus BK
Questo virus può essere diagnosticato tramite un esame del sangue per BKV o un test urinario per cellule decoy, oltre a eseguire una biopsia nei reni. Le tecniche PCR vengono spesso utilizzate per identificare il virus.
Trattamento dell’infezione da virus BK
Il pilastro della terapia è la riduzione dell’immunosoppressione. Un recente aumento di BKVAN è correlato all’uso di potenti farmaci immunosoppressori, come tacrolimus e micofenolato mofetile (MMF). Gli studi non hanno mostrato alcuna correlazione tra BKVAN e un singolo agente immunosoppressore, ma piuttosto il carico immunosoppressivo totale.
- Non esistono linee guida o livelli e dosi di farmaci per la corretta riduzione degli immunosoppressori in BKVAN
- I metodi più comuni:
- Ritiro di MMF o tacrolimus
- Sostituzione del tacrolimus con ciclosporina
- Riduzione del carico immunosoppressivo generale
- Alcuni livelli di ciclosporina sono riportati ridotti a 100-150 ng/ml e livelli di tacrolimus ridotti a 3-5 ng/ml
- Un’analisi retrospettiva di 67 pazienti ha concluso che la sopravvivenza dell’innesto era simile tra riduzione e interruzione degli agenti.
- Uno studio monocentrico ha mostrato che gli innesti renali erano preservati in 8/8 individui gestiti con riduzione della immunosoppressione, mentre la perdita dell’innesto si è verificata in 8/12 pazienti trattati con un aumento della terapia per quella che si pensava fosse un rigetto d’organo.
Altre opzioni terapeutiche includono Leflunomide, Cidofovir, IVIG e fluoroquinoloni. Leflunomide, un inibitore della sintesi delle pirimidine, è ora generalmente accettato come la seconda opzione terapeutica dopo la riduzione dell’immunosoppressione.
Leflunomide in BKVAN
Il razionale dell’uso di leflunomide in BKVAN deriva dalle sue proprietà immunosoppressive e antivirali combinate. Due studi composti da 26 e 17 pazienti che hanno sviluppato BKVAN in un regime di tre farmaci di tacrolimus, MMF e steroidi hanno sostituito il MMF con leflunomide a dosi di 20-60 mg al giorno. L’84% e l’88% dei pazienti rispettivamente hanno mostrato clearance o una riduzione progressiva del carico virale e una stabilizzazione o miglioramento della funzionalità dell’innesto. In uno studio condotto da Teschner et al. nel 2009, 12/13 pazienti che avevano scambiato il MMF con leflunomide hanno eliminato il virus entro 109 giorni. In una serie di casi, si è osservato un miglioramento o una stabilizzazione in 23/26 pazienti con BKVAN dopo la sostituzione di MMF con leflunomide.
Non esistono linee guida per il dosaggio di leflunomide in BKVAN. La variabilità da paziente a paziente ha reso difficili il dosaggio e il monitoraggio di leflunomide.
- Negli studi di 26 e 17 pazienti, le dosi variavano tra 20 mg/giorno e 60 mg/giorno con livelli di picco di 50—100 µg/ml. Il fallimento è stato visto in pazienti con livelli plasmatici di leflunomide < 40 µg/ml.
- Uno studio di 21 pazienti ha trovato che i livelli bassi (< 40 µg/ml) e i livelli alti (> 40 µg/ml) avevano effetti simili sulla velocità di clearance virale. Quelli con livelli più alti hanno avuto più eventi avversi (ematologici, epatici).
- Nello studio di Teschner et al., i dosaggi e le concentrazioni del farmaco non hanno mostrato correlazione con variazioni sostanziali da persona a persona.
- Nello studio di Teschner, basse concentrazioni del farmaco erano associate a una riduzione del carico virale. Questo rende difficile determinare se la riduzione del carico virale o l’aggiunta di leflunomide fosse la causa della clearance virale.
Altre opzioni di trattamento
- Antibiotici chinolonici: Ciprofloxacina (Cipro) ha dimostrato di ridurre significativamente i carichi virali ma non ci sono dati sulla sopravvivenza e sulla perdita dell’innesto.
- Immunoglobulina endovenosa (IVIG) ha uso nel trattamento dell’infezione e del rigetto dell’innesto — difficile da distinguere
- Cidofovir ha dati limitati ed è altamente nefrotossico.
Storia
Il virus BK fu isolato per la prima volta nel 1971 dall’urina di un paziente trapiantato renale, iniziali B.K. Il virus BK è simile a un altro virus chiamato virus JC (JCV), poiché i loro genomi condividono il 75% di somiglianza nella sequenza. Entrambi questi virus possono essere identificati e differenziati tra loro eseguendo test sierologici utilizzando anticorpi specifici o utilizzando un approccio di genotipizzazione basato su PCR.